医薬品の安全対策
副作用情報の収集
1961年のサリドマイド薬害事件が契機となり、1968年WHO加盟各国を中心に副作用を収集評価する体制「WHO国際医薬品モニタリング制度」確立。
WHO加盟国の一員である日本の制度が「医薬品・医療機器等安全性情報報告制度」。
医薬品・医療機器等安全性情報報告制度は、医薬品の副作用と疑われる健康被害が発生した時に、厚生労働大臣に報告しなければならないという制度です。ちなみに実務上は、(独)医薬品医療機器総合機構に提出します。
副作用・感染症報告制度(企業→厚生労働大臣)
企業→厚生労働大臣(実務上は(独)医薬品医療機器総合機構)
副作用症例報告/感染症用例報告/外国での措置報告/研究報告
がある。
感染症定期報告制度(企業→厚生労働大臣)
生物由来製品(血液製剤等)を製造販売企業は、その製品について常に安全性を評価して、
企業→厚生労働大臣(実務上は(独)医薬品医療機器総合機構)
※生物由来製品については、人または生物の組織などを原材料としていることから、常に危害発生の原因となり得るとのことで前出の「副作用・感染症報告制度」に加え定期報告がの制度がある。
製造販売業社が行う情報収集への協力(医薬関係者→企業)
薬局開設者・医療施設の開設者・医薬品の販売業社・医師・薬剤師・その他医薬関係者(登録販売者を含む)は製造販売業社が行う情報収集に協力するように努めなくてはならない。
医薬品の副作用等による健康被害の救済
医薬品副作用被害救済制度
副作用による被害者の迅速な救済を図るための製薬企業の社会的責任に基づく公的制度。
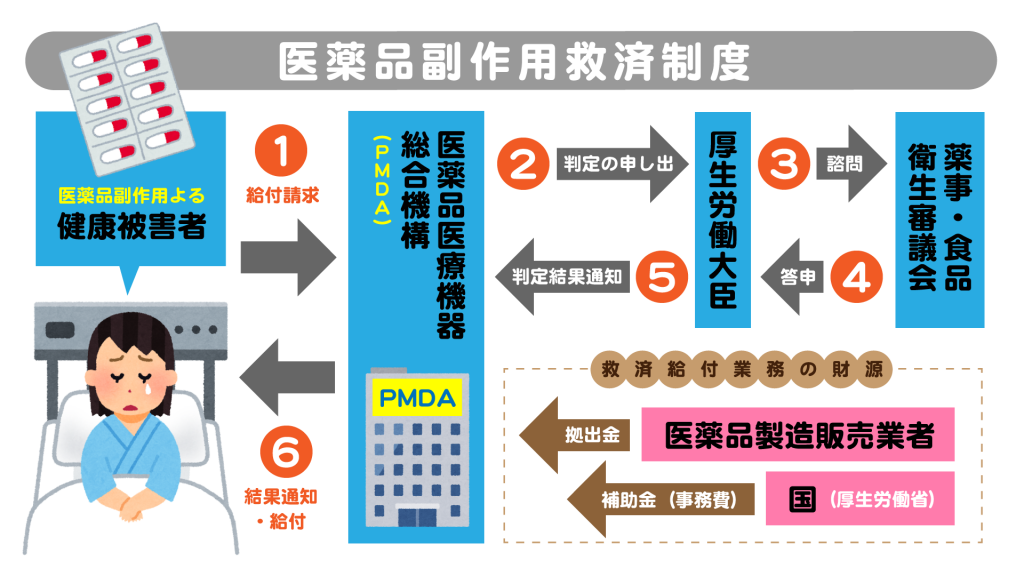
救済給付業務の財源
給付費——–製造販売業社から年度ごとに納付される拠出金が充てられる。
事務費——–事務費の2分の1相当額が国庫補助により賄われる。
総合機構の関連業務
◉生物由来製品感染等被害救済制度
生物由来製品は。医薬品副作用救済制度の対象外となっており、生物由来製品感染等被害救済制度が設けられています。
◉和解が成立したスモン患者の健康管理手当てや介護費用の支払い業務
◉血液製剤によるHIV感染者・発症者に対する健康管理費用の支給((公財)友愛福祉財団からの委託)
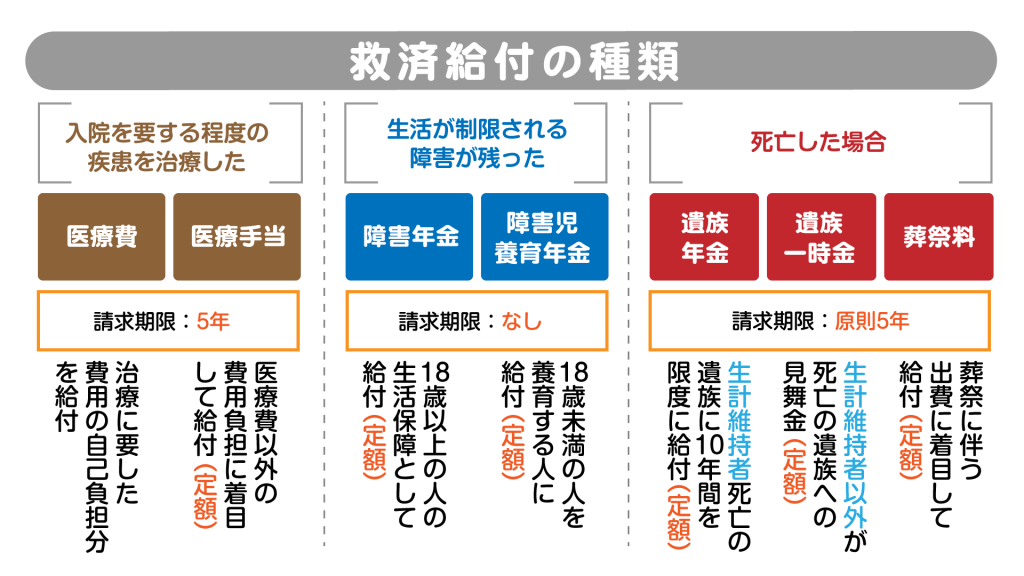
救済給付の種類
医薬品副作用被害救済制度についての動画です。